¿Deberían vacunarse contra el coronavirus las embarazadas y madres lactantes? A pocos días de que empiece la campaña de vacunación contra la Covid 19 ya empiezan a surgir dudas y preguntas relacionadas con la vacuna…

La vacuna española contra el coronavirus Bimervax, desarrollada por la empresa española Hipra, ha sido autorizada por la Agencia Europea del Medicamento.
Bimervax ha mostrado ser, al menos, tan eficaz como Comirnaty para restablecer la protección frente a la COVID-19 en personas a partir de los 16 años.
Bimervax se evaluó como parte de OPEN, una iniciativa que comenzó en diciembre de 2020 con el objetivo de aumentar la colaboración internacional en la revisión de la UE de vacunas y terapias COVID-19.
Aprobada la vacuna española contra el coronavirus Bimervax
La Autoridad Europea de Medicamentos (EMA, por sus siglas en inglés) ha aprobado Bimervax, la vacuna española contra el coronavirus desarrollada por la empresa española Hipra, destinada a combatir el SARS-CoV-2, como refuerzo para personas mayores de 16 años que previamente hayan sido vacunadas con vacunas de ARNm (ARN mensajero).
La EMA comenzó la evaluación científica de esta vacuna el 29 de marzo de 2022, aunque su aprobación se esperaba para mediados del año anterior. El Comité de Medicamentos de Uso Humano (CHMP, por sus siglas en inglés) de la EMA, formado por expertos de los diferentes Estados miembros de la UE, entre ellos la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS), ha completado su evaluación, concluyendo por consenso que dispone de datos suficientemente sólidos sobre su calidad, seguridad y eficacia; es decir, que el balance beneficio/riesgo es positivo.

El principal estudio realizado con Bimervax es un ensayo clínico que comparó la respuesta inmunitaria desencadenada por esta nueva vacuna con la desencadenada por la vacuna de ARNm autorizada Comirnaty, de BioNTech/Pfizer contra SARS-CoV-2 en su variante original (Wuhan). Este ensayo recibió el visto bueno de la AEMPS el pasado 1 de febrero de 2022. En este estudio participaron 765 adultos que ya habían completado la vacunación primaria con 2 dosis de Comirnaty y luego recibieron una dosis de refuerzo de Bimervax o Comirnaty.
A pesar de que Bimervax generó niveles de anticuerpos más bajos contra la cepa original del SARS-CoV-2 en comparación con Comirnaty, produjo niveles más altos de anticuerpos frente a las variantes beta y ómicron, así como niveles similares contra la variante delta.
Además, para su evaluación, se han presentado datos de otro ensayo clínico que incluyó a 36 adolescentes de 16 a 17 años, con datos de respuesta inmune disponibles para 11 de ellos. El estudio concluyó que Bimervax administrado como refuerzo produce una respuesta inmunitaria adecuada en estos adolescentes, con una producción de anticuerpos comparable a la observada en adultos (de 18 años o más) que recibieron Bimervax.
Adicionalmente, se han llevado a cabo otros ensayos clínicos autorizados por la AEMPS: el 11 de marzo de 2022 se autorizó un segundo ensayo clínico fase IIb para recabar datos adicionales de seguridad y observar cómo actúa frente a ómicron en voluntarios que han recibido 2 dosis de Vaxzevria (AstraZeneca) y una dosis de refuerzo de Hipra, frente a aquellas personas que han sido vacunadas con dos dosis de Vaxzevria y Comirnaty.
Es segura y eficaz
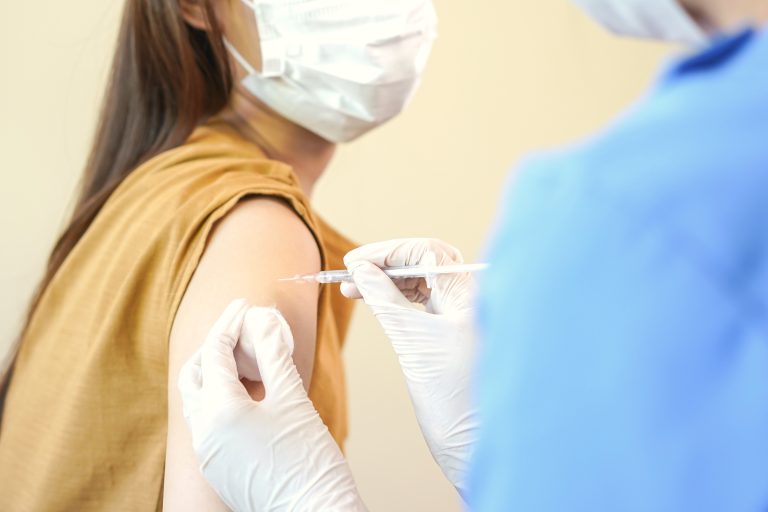
El CHMP ha concluido que se espera que una dosis de refuerzo de Bimervax sea al menos tan eficaz como Comirnaty para restablecer la protección frente a la COVID-19 en personas a partir de los 16 años.
Por otra parte, el perfil de seguridad de Bimervax es comparable al de otras vacunas frente a la COVID-19. Los efectos secundarios más comunes observados fueron los ya observados anteriormente: dolor en el lugar de la inyección, dolor de cabeza, cansancio y dolor muscular. Estos efectos desaparecieron pocos días después de la vacunación.
«Por lo general, estos fueron de leves a moderados y desaparecieron unos pocos días después de la vacunación. La seguridad y eficacia de la vacuna continuarán siendo monitorizadas a medida que la vacuna se use en toda la UE a través del sistema de farmacovigilancia europeo y estudios adicionales por parte de la empresa y las autoridades competentes», destacan desde la EMA
En relación a esto, Hipra está obligada a proporcionar actualizaciones periódicas de seguridad.
La primera vacuna contra el Covid-19 desarrollada y fabricada en Europa
La Comisión Europea (CE) será ahora la responsable de otorgar la autorización de comercialización para que esta vacuna pueda distribuirse en todos los Estados miembro de la UE, como sucede con el resto de medicamentos autorizados por procedimiento centralizado.
En agosto de 2022, la empresa firmó un acuerdo de adquisición conjunta por el que 13 estados miembros de la UE, entre ellos España, tienen la opción de comprar hasta 250 millones de dosis de la vacuna.
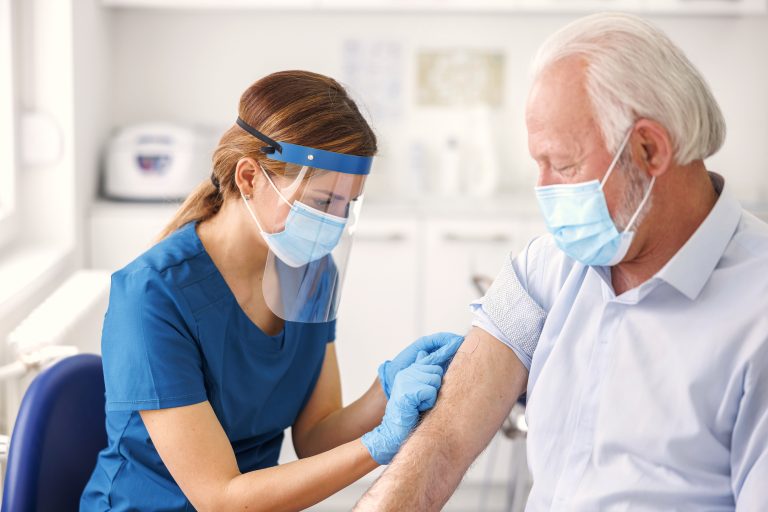
El consejero delegado de Hipra, David Nogareda, remarcó que esta era la «primera y única» vacuna contra el Covid-19 diseñada, desarrollada y fabricada íntegramente en Europa, por lo que pensaba que jugará un papel importante en los planes de vacunación de España, Europa y el mundo, ha dicho.
El hito de la vacuna Bimervax
Se espera que Bimervax «tenga una eficacia y seguridad similar a las demás vacunas«, afirma a «Science Media Centre España» (SMC) Margarita del Val, viróloga e inmunóloga en el Centro de Biología Molecular Severo Ochoa y coordinadora de la Plataforma de investigación interdisciplinar en Salud Global del CSIC.
«Es un hito tener autorizada la primera vacuna para uso humano derivada de la investigación y desarrollada por una empresa española. No tener ninguna hasta ahora no era acorde al nivel y potencia del país. La nueva vacuna Bimervax, de Hipra, es algo distinta y original en su composición comparada con todas las demás vacunas frente al coronavirus que están autorizadas en la Unión Europea por la Agencia Europea del Medicamento, ocho con esta», sostiene la experta.
Pero «a la vez, usa un método clásico en la producción de vacunas, al contener proteínas como las del virus», por lo que se espera que tenga una eficacia y seguridad similar a las demás, incide la especialista.
«Es una inversión para el futuro del país. Seguimos investigando y desarrollando vacunas porque siguen haciendo falta más y mejores vacunas: para este virus, para otras infecciones respiratorias, para otros agentes infecciosos, actuales o futuros. Vacunas que nos protejan también de la infección y, por tanto, permitan la inmunidad colectiva si evitan que los vacunados contagien; son las vacunas que mejor atajan pandemias y que permiten recuperar la normalidad más rápido. Vacunas más estables, más fáciles de conservar, más baratas. Vacunas más fáciles de inocular, que no requieran personal especializado; vacunas que, por esas ventajas, lleguen al último rincón del planeta», incide Del Val.
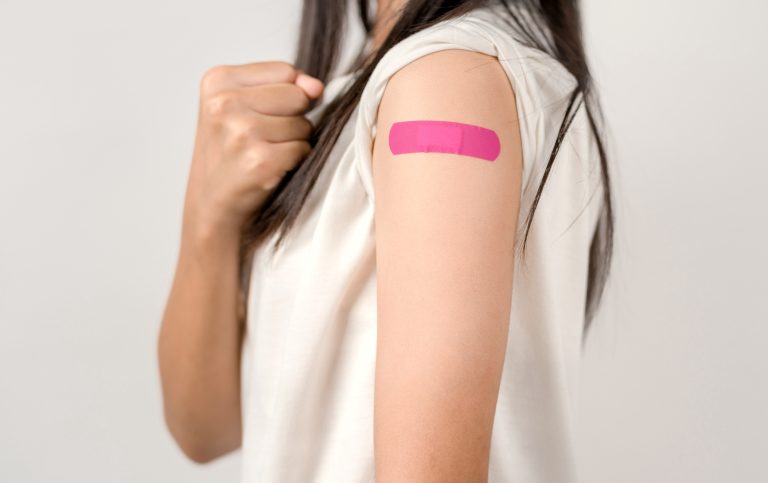
Por su parte, José Gómez Rial, inmunólogo del Hospital Clínico Universitario de Santiago indica a SMC que «siempre es una buena noticia que se apruebe una nueva vacuna que se añada a las ya existentes en la lucha frente a la Covid-19″. Eso sí, el experto advierte que «se tiene que demostrar que aún es mejor que las ya existentes, no hay evidencia científica para afirmar tal cosa».
Aunque el especialista lamenta «enfriar un poco las expectativas que se han creado con Hipra y las declaraciones de la ministra en este sentido», manifiesta estar seguro de que la nueva vacuna dará muy buenos resultados.
«Estoy convencido que se obtendrán muy buenos resultados con ella. Especialmente debería indicarse esta vacuna, que emplea una plataforma diferente, para aquellas personas que no hayan respondido de forma eficiente a la pauta inicial con una vacuna de ARNm y, por tanto, aprovechar las ventajas de una combinación heteróloga, que tan buenos resultados ha demostrado hasta el momento», añade el experto.
¿Cómo funciona Bimervax?
En su composición, la nueva vacuna contra el coronavirus es diferente a las que ya están autorizadas por la EMA. Bimervax contiene una proteína recombinante basada en las variantes Beta y Alfa del SARS-CoV-2. Se trata de la primera vacuna con estas características autorizada en la Unión Europea contra el virus.
Desde la EMA explican que esto significa que la vacuna contiene información para inducir una respuesta en forma de anticuerpos contra las 2 variantes de la Covid-19. Además, este antígeno se acompaña de un adyuvante, sustancia que aumenta la respuesta inmune.

Bimervax se conserva a temperatura refrigerada entre 2ºC y 8ºC. Hipra destaca la vacuna ya está «lista para utilizar, es decir, no es necesario reconstituirla antes de su uso, facilitando así la tarea al personal sanitario».
Por su parte, Gómez comenta que la tecnología empleada por Hipra «no permite una rápida adaptación a los cambios del virus. En este sentido, siempre es más flexible y rápida la tecnología del ARNm, y precisamente es una de sus ventajas con respecto a las existentes hasta ahora».
Si quieres más información sobre esta u otras vacunas o necesitas asesoramiento profesional sobre el covid y sus síntomas, en la Tribu CSC puedes consultar online a nuestro equipo de expertos/as en salud materno-infantil y crianza respetuosa. Entre ellos/as se encuentra la pediatra Gloria Colli, la matrona Sara Caamaño y el enfermero de pediatría Armando Bastida.















0 responses on "La Agencia Europea del Medicamento aprueba la vacuna española contra el coronavirus Bimervax"